反応式はクエン酸中のカルボン酸1つと炭酸水素ナトリウム中のナトリウムが反応して,クエン酸ナトリウムと水,二酸化炭素が生成します. 反応式(式中の数字は全て下付き文字 クエン酸中のは結合の手を示しています.) HOOCCH2CH (OH) (COOH)CH2COOH化学反応式の書き方 例1 水素の燃焼・・・水素+酸素→水 化学式・・・水素 (H2),酸素 (O2),水 (H2O) まず、水素+酸素→水をモデルと化学式で表す 両辺原子の数を数える 左辺のOが2個、右辺が1個なので右辺の水分子を増やす 右辺の物質は水なので、酸素構造式 ニオイの表現「ウッディーなラベンダー様香気」 C.構造異性体によるニオイの違い 構造異性体というのは、分子式が同じでも構造式が異なるものをいいます。例えば、C4H10(ブタン)では、構造式が図のように2種類考えられます。

次氟酸 维基百科 自由的百科全书
硝酸 酸 化学式
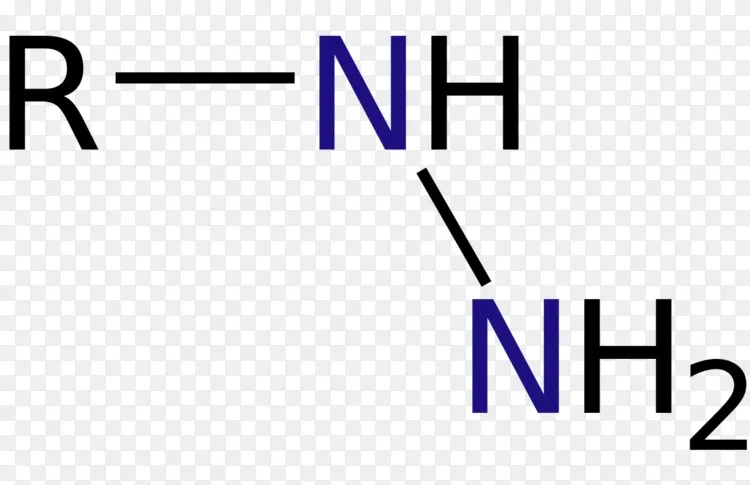
硝酸 酸 化学式- アミノ酸を分類しながら覚えよう 高校化学で習う「αアミノ酸」の基本構造は、 以下の通りです。 この基本構造のrが変化することで、 αアミノ酸は約種類もあります。 これをすべて丸暗記するのは厳しいので、 まず、日本語で化学反応式を書いてみよう! ① 酸化銀 → 銀 酸素 (慣れたら省略していいよ。 ) 次に、①の日本語を化学式にそれぞれ変えるよ。 ② Ag2O → Ag O2 だね。 これで完成にしたいけれど、 Ag2O → Ag O2 → + のままでは、 矢印の左と右で原子の数が合っていない ね。 この場合は 両側で原子の数を合わせないといけない んだよ。 それでは係数をつけて、 原子の個数



水杨酸 简介 作用 危害 结构式 化学式 毒理 合成 范德生物科技公司
カルボン酸の分類 分類 名称 化学式 融点(℃) 備考 飽和 モノカルボン酸 ギ酸 hcooh 8 アリの体内で発見された 酢酸 ch 3 cooh 17 食酢の主成分 プロピオン酸 ch 3 ch 2 cooh ー21 乳製品によく含まれる 酪酸(らくさん) ch 3 ch 2 ch 2 cooh ー5 バターの成分 「化学式」とは、ある物質の成り立ちを原子の記号と数字で表した式 のことをいいます。 「原子の記号」は「 元素記号 」とも呼ばれ、酸素や水素などをアルファベットで表します。 定義だけ聞くと難しいように感じますが、普段の生活の中で当たり前のように存在している 水や空気、金属なども化学式で表すことができる のです。 そしてこの化学式は、大きく分けて「 組成式 」 過マンガン酸カリウムの性質と用途 過マンガン酸カリウムの化学式はKMnO 4 で、Mnの酸化数は(VII)です。 Mnの電子構造はAr3d 5 4s 2 なので、Arと同じ電子配置である(VII)の状態がMnの最高酸化数と考えられています。 高い酸化数を有しているため、自身は化学反応によって還元されやすい状態です。
化学式はHOOC・(CH 2 ) 2 ・CH(NH 2 )・COOH。 アミノ酸の一種。 Lグルタミン酸はタンパク質中に広く存在し,特に穀類のタンパク質に多い。 無色の粉末で,約100倍の水に溶ける。 アミノ基移転反応など窒素代謝一般に重要な役割を占めるとともに,高等動物の中枢神経系では神経伝達物質としても働いている。 またこのナトリウム塩は コンブ の うまみ の 主成分 として知られる。 → クエン酸ナトリウムの化学式 クエン酸はカルボン酸であり、カルボキシ基(COOH) を持ちます。 このカルボキシ基が、水中ではいくらかの割合で水素イオン(H )を手放すため、クエン酸水溶液は酸性なのです。 クエン酸はカルボキシ基が3つある、3価のカルボン酸です。 このため、分子内の3つの部分で塩基(アルカリ)と反応します。 3つのカルボキシ基のうち、いくつがナ アミノ+酸 アミノ基「NH 2 」: アミノ カルボキシ基「COOH」: 酸 アミノ酸の「アミノ」は、アミノ基「NH 2 」をもっているところからきています。 アミノ基とは、アンモニアから水素Hを取り除いたもので、NH 2 であらわされます。 アミノ酸の「酸」は、「酸性」のことです。 一般に、酸性を示す有機化合物の多くは、カルボキシ基「COOH」を含んでいます。 つまり
酸和盐反应的化学方程式 1酸与盐反应的化学方程式(NH 4 ) 2 SO 4 K 2 CO 3 = K 2 SO 4 2NH 3 ↑ H 2 O CO 2 ↑AlCl 3 3Na 2 CO 3 6H 2 O = 2Al(OH) 3 ↓3CO 2 ↑6NaClAl 2 (SO 4 ) 3 6NaHCO 3 = 2Al(OH) 3 ↓ 6CO 2 ↑3Na 2 SO 4AlCl 3 3NaAlO 2 6H 2 O = 4Al(OH) 3 ↓ 3NaCl2HClCaCO3=CaCl2H2OCO21大理石与稀盐酸反サリチル酸(サリチルさん、英 salicylic acid )は、 ベータヒドロキシ酸 (英語版) の一種の植物ホルモン。 化学合成も比較的容易である。消炎鎮痛作用、皮膚の角質軟化作用があり医薬品としてはイボコロリやウオノメコロリで知られ 、洗顔料などにも配合される 。1/121 覚えたい元素記号と化学式 何度も繰り返して覚えよう! 元素記号 は原子番号を示す。 44!これだけ覚えれば,大学入試も完璧です。 1水素 H 2ヘリウム He 3リチウム Li 4ベリリウム Be 5ホウ素 B 6炭素 C 7窒素(チッ素) N 8酸素 O 9フッ素 F



树脂化学式 醇化学式 菲化学式 大山谷图库 手机版



氢氟酸防腐材料 氢氟酸的化学式是什么 怎么防氢氟酸腐蚀
酸化とは、物質が酸素とくっついて新たな化合物ができることで、物を燃やす時も酸化反応が起きています。 BBQの炭を燃やした時を考えてみましょう。 炭は炭素ですから化学式はCですね。 まずは、化学反応を文字であらわすと 「炭素 + 酸素 → 二酸化炭素」 になります。 次にこれを化学式に置き換えて書くと、 「C+O2 → CO2」となります。 これが今回のテーマの化学反応式になります。 化化学反応式35両性元素の単体と酸との反応 2Al 6HCl → 2AlCl_{3} 3H_{2} 両性元素であるアルミニウムAlと酸であるHClが反応すると 塩 と 水素H 2 が生成する。CO2H2O=H2CO3 酸在生活中广泛存在,请将你所知道的酸的化学式(1)用名称填入下列相应的横线上(1)食醋中含有—— (2)瓶装汽水中含有——(3)胃液中含有——(4)汽车用铅蓄电池中含有—— (1)醋酸(或称乙酸




水泥化学式专用硅酸盐 硅酸盐水泥白色 Buy 水泥 特种硅酸盐水泥化学式product On Alibaba Com



化学物质分子化学式大黄酸png图片素材免费下载 图片编号 Png素材网
クエン酸回路の全体の反応式 クエン酸回路とは、アセチルcoaを反応の起点としたエネルギー生産のための反応系です。 この反応系によって、1個の「gtp」、3個の「nadhh 」、1個の「fadh 2 」がつくられます。 クエン酸回路の反応式まとめ(簡易版) 化学反応式は名前のとおり化学式の反応を表した式です。 2,クエン酸,重曹,水の化学式,化学反応式 化学式 ・クエン酸→C6H8O7 ・重曹→NaHCO3 ・水→H2O 化学反応式 クエン酸+炭酸水素ナトリウム→クエン酸三ナトリウム+水+二酸化炭素 C6H8O73NaHCO3→ Na3C6H5O7 3CO2 3H2O となります。 4人がナイス! しています ナイス! ID非公開 ID非公開さん 質問 酸の価数 とは、 酸1分子が出しうる水素イオンHの数 のことであり、 塩基の価数 とは 塩基1化学式が出しうる水酸化物イオンOH-の数または受けとることができる水素イオンHの数 のことです。 価数の覚え方としては、酸・塩基の化学式およびイオンの形を覚えることが最もベストです。 HClは化学式中にHを1つもっているので1価の酸、Ca (OH) 2 は化学式中に2つのOHをもって



己二酸的结构式及化学式是什么 16己二酸化学式 恩芝网



草酸 乙二酸 草酸是什么 价格 化学式 作用 恒亿化工
炭酸水が化学的に何でできているか教えてください。wikipediaとかで自分でいろいろと調べて、周りの人に質問したのですが、結局、1)H2OとCO22)H2OとH2CO33)H2CO3がHとHCO3 に分かれ、HCO3 がHとCO3 2に分かれるから、H2Oと 七、酸、碱、盐1、酸的化学性质(1)酸金属盐氢气(见上)(2)酸金属氧化物。 化学方程式的计算首先要设未知数;其次写化学反应方程式,在已知质量的物质下方,竖着分别写出相对分子质量。 化学方 程 式是用 化学式来表示 化 学反应的 式子。苯甲酸:C6H5COOH 氢氟酸:HF 氢溴酸:HBr 氢硫酸:H2S 氰酸:HOCN 高锰酸:HMnO4 高氯酸:HClO4 氯酸:HClO3 次氯酸:HClO



丁酸戊酯 Amyl Butyrate 540 18 1 参数 分子结构式 图谱信息 物竞化学品数据库 专业 全面的化学品基础数据库
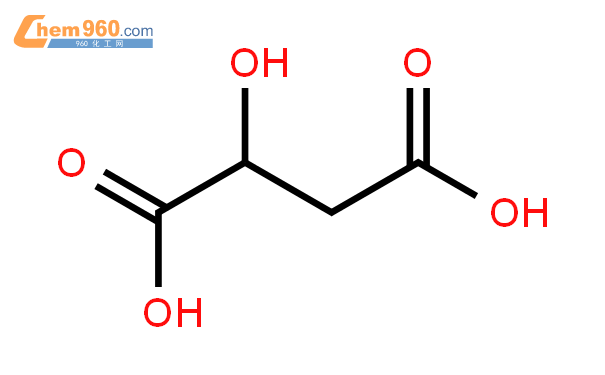



苹果酸结构式 苹果酸化学式 960化工网
フッ化水素酸(HF)の化学式、構造、性質および用途 の フッ酸 (HF)フッ化水素が溶けている水溶液です。 この酸は主に濃硫酸と鉱物蛍石(CaF)との反応から得られる。 2 )ミネラルは酸の作用によって分解され、残りの水はフッ化水素ガスを溶かし化学式の作り方 化学式の仕組みが分かったら実際に自分で作ってみましょう。ポイントは 各元素が持っている結合できる「手の数」です。 例えば水素は手を1本、酸素は手を2本、窒素は手を3本、炭素は手を4本持っています。 硫酸酸性の過マンガン酸カリウムと硫酸鉄(Ⅱ)の酸化還元反応の化学反応式を作りながら、この3つの段階を確認します。 ちなみに 硫酸酸性とは硫酸を使って酸性にした水溶液という意味 です。 後で重要になるので意味を理解しておきましょう」 ②




乙二酸乙二酯化学式 乙二酸乙二酯的化学式怎么写 三人行教育网 Www 3rxing Org



对硝基苄醇丙二酸单酯有什么性质 河南丘化化工科技有限公司
パルミチン酸を水酸化ナトリウム(苛性ソーダまたはアルカリ液)で鹸化して、パルミチン酸ナトリウム塩を形成する。パルミチン酸ナトリウムの化学式はcです。 16 h 31 nao 2 セチルアルコールまたはパルミチルアルコールもパルミチン酸から得られる。今回は、脂肪酸の完全酸化における H 2 O の関与について考察してみます。 炭素数 16 の脂肪酸であるパルミチン酸を例にして、先ず、その化学的な燃焼を考えます。 その反応式は次のようになります。 C 16 H 32 O 2 23 O 2 → 16 CO日本大百科全書(ニッポニカ) ステアリン酸の用語解説 生体内にみいだされる高級飽和脂肪酸の一種で、c17h35coohの化学式をもつ。分子量2845、融点696℃。常温で白色の葉状結晶。他の高級脂肪酸と同様に、水に不溶、有機溶媒に可溶。グリセリドを構成するさまざまの脂肪酸のなかの主要成分




苯甲酸化学式分子羧酸png图片素材免费下载 图片编号 Png素材网



乙醇化学式是啥乙醇化学式
化学上,电离时生成的阳离子全部是氢离子(H)的化合物叫做酸,或者溶于水并能释放质子形成H3O(水合氢离子)的物质也是酸。 H3O的浓度越高,溶液酸性越强。 即使是纯水中也存在H3O,其浓度为107mol/L。 这是由于质子从一个水分子跑到另一个水分子所造成的。 在传统意义上,H3O的浓度还取决于氢离子的浓度,虽然水溶液中的大部分氢离子是以H3O形式存在的。 酸的分类: 1、根 オレイン酸 分子式C 17 H 33 COOH 全炭素数18 官能基COOH1コ 炭化水素基長い、不飽和、C=C1コ(cis型) 高級脂肪酸一覧 高級脂肪酸の融点 飽和脂肪酸の場合 飽和脂肪酸は 炭素数が増加するにつれて融点が上昇 する。 これは、炭素数が増えると分子量が大きくなるため、分子間に働く引力が強くなるためである。 不飽和脂肪酸の場合 不飽和脂肪酸は飽和脂肪酸に 氧硅的化学式为si三氧化二铝学式为al2o3故sio2alo3 据相对重量为成分子各原的相对子量量之和, 可得al2o的相对分子量为27*216*3=102, 填12。 有机酸是指一些具有酸性的有机化合物*常见的有机酸是羧酸, 其酸性源于羧基 cooh磺酸 so3h亚磺酸rsooh硫羧酸rcosh。




分子化学物质化学式麦角酸化学名称物理结构png图片素材免费下载 图片编号 Png素材网




生石灰化学式 生石灰和熟石灰的化学名称 环球信息网
硫酸:H2SO4、盐酸:HCl、硝酸:HNO3、磷酸:H3PO4、醋酸:CH3COOH、亚硫酸:H2SO3、苯甲酸:C6H5COOH、氢氟酸:HF、氢溴酸:HBr氢硫酸:H2S、氰酸:HOCN、高锰酸:HMnO4、高氯酸:HClO4。 1 酸 电离时生成的阳离子全部是氢离子 (H)的化合物叫做酸,或者溶于水并能释放质子形成H3O (水合氢离子)的物质也是酸。 H3O的浓度越高,溶液酸性越强。 即使



安徽专版中考化学复习方案课时训练10化合价与化学式物质的分类试题 无忧文库




乙二酸乙二酯化学式 乙二酸乙二酯的化学式怎么写 三人行教育网 Www 3rxing Org



酸醋的化学式醋酸的化学式是什么 欧星推网
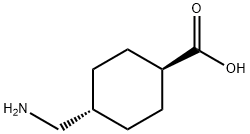



氨甲环酸 1197 18 8
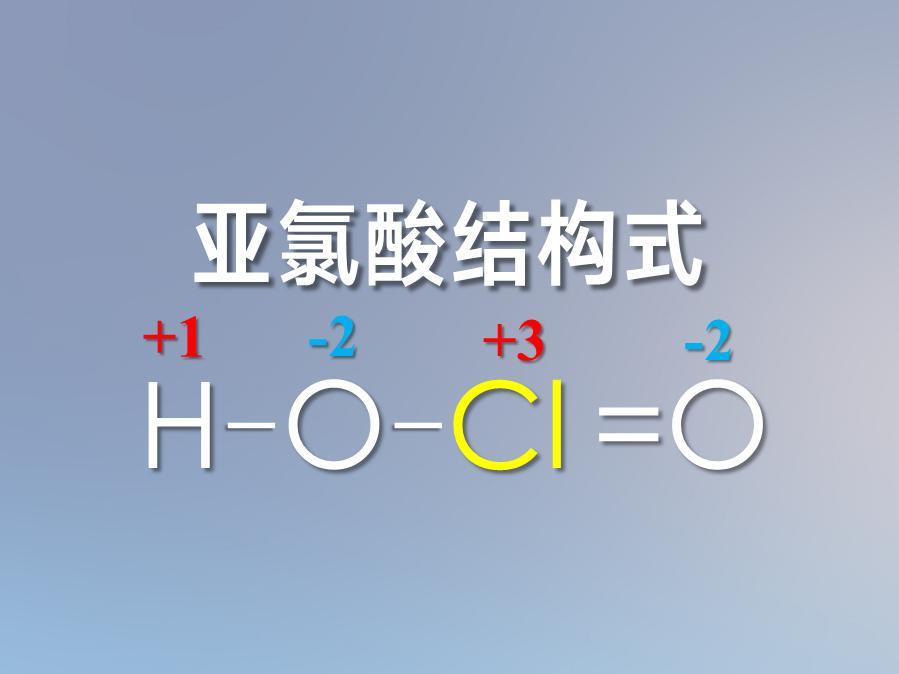



亚氯酸 搜狗百科



月桂酸化学式肉豆蔻酸异丙酯危害硬脂酸镁气相 朵拉利品网



对甲苯酸 对甲苯酸化学式化学物质png图片素材免费下载 图片编号 Png素材网



甲酸化学式怎么写 育才学习网



牛磺酸 Msds 用途 密度 牛磺酸cas号 107 35 7 化源网




柠檬酸无水物化学式制造 Buy 篷栗 Citrique一水柠檬酸无水柠檬酸acido Citrico Ttca 少尉 Rzbc 中粮集团 Cofco 联合bp98 Fcc 30柠檬酸钠一水柠檬酸8 80目无水柠檬酸 30 100目 无水柠檬酸化学式制造
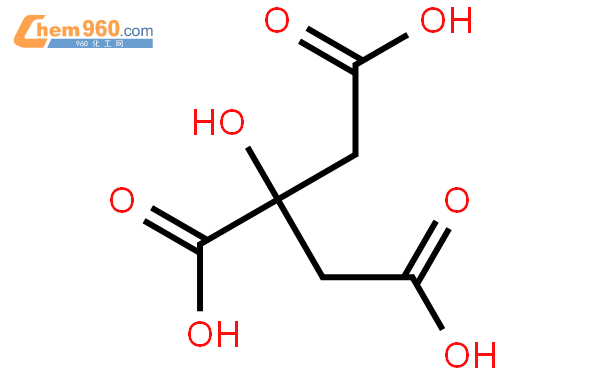



柠檬酸结构式 柠檬酸化学式 960化工网



亚氯酸盐化学式亚氯酸及亚氯酸盐的用途 我有车



琥珀酸 Wikiwand



酸化学式 乙醇化学式 碳化学式 大山谷图库 手机版



苏打化学式 臭氧化学式 氧气化学式 第16页 大山谷图库 手机版



草酸 乙二酸 草酸是什么 价格 化学式 作用 恒亿化工



无氧酸化学式 初三网
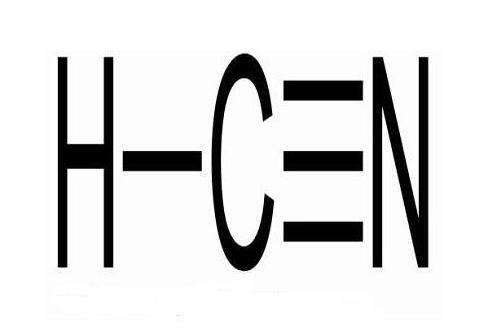



氰化氢 化学物质 搜狗百科



初中常见酸碱盐化学式 初三网



柠檬酸的化学式和结构式是什么 作业帮
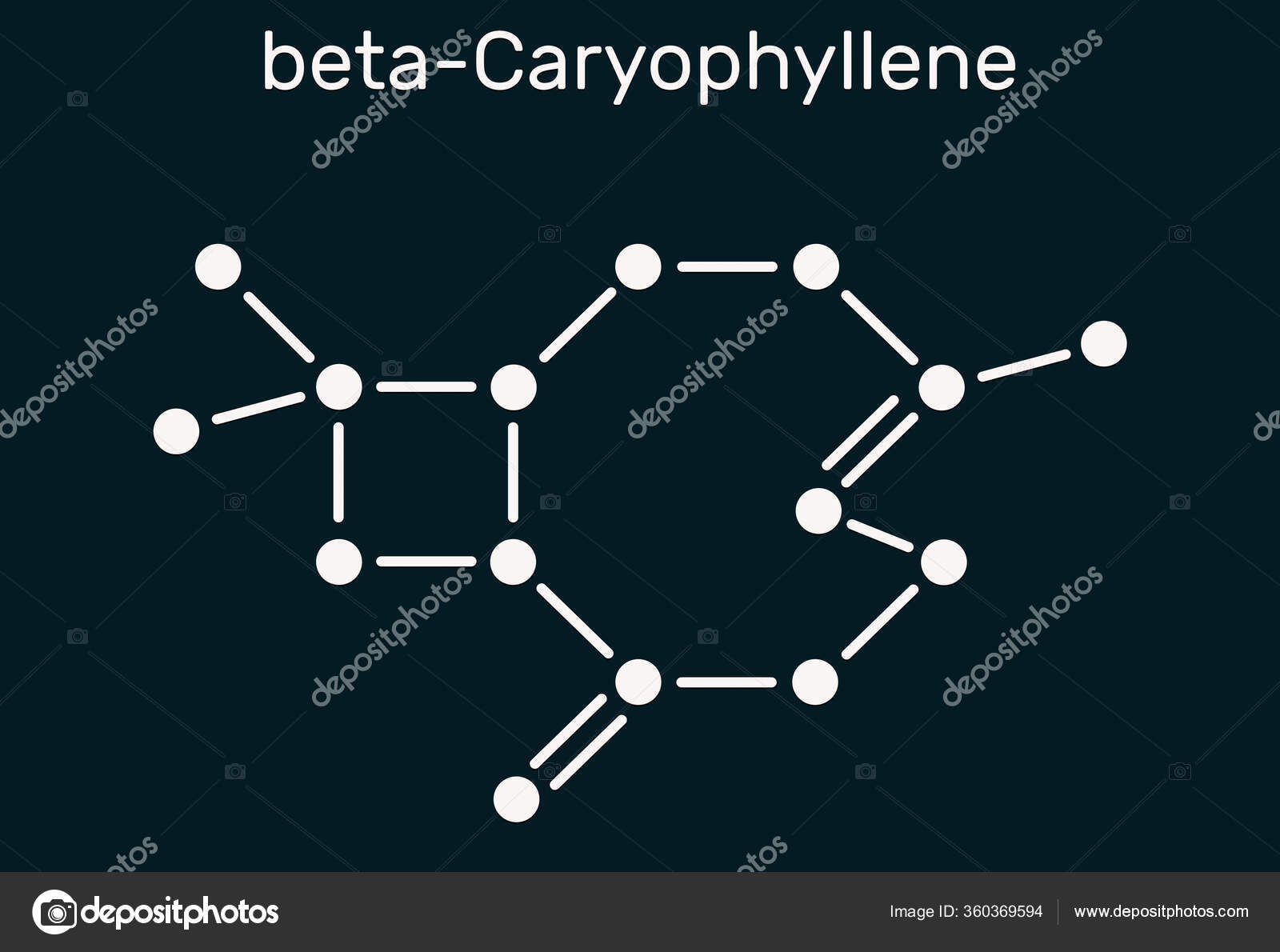



叶绿素叶绿素c15h24分子许多香精油的成分是天然的双环倍半胱氨酸深蓝色背景上的结构化学式说明1 图库照片 C Avk97 Yandex By
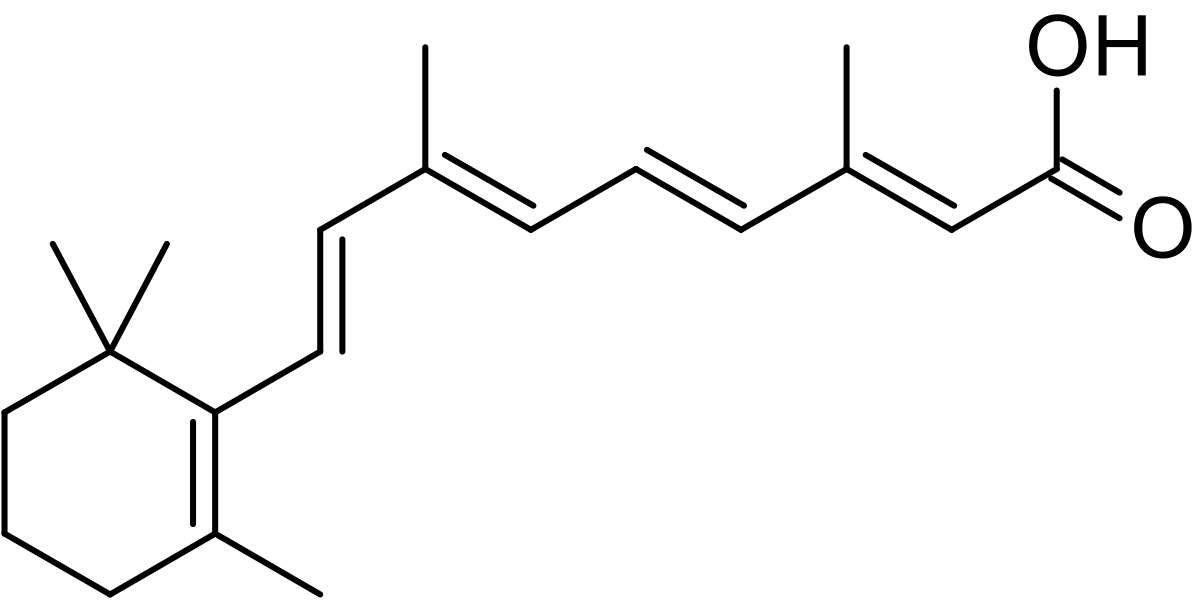



維a酸 维基百科 自由的百科全书
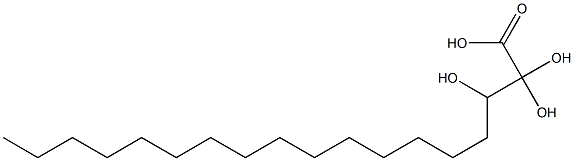



三羥硬脂酸cas 三压硬脂酸分子式 力太网




三酸甘油酯 Wikiwand



葡萄糖酸钠 工业葡萄糖酸钠价格 特性 化学式 恒亿化工




鞣花酸 维基百科 自由的百科全书



柠檬酸cas 77 柠檬酸结构 Urpimp网



次氟酸 维基百科 自由的百科全书




高锰酸钾化学式高锰酸钾的化学式




柠檬酸一水合物 无水柠檬酸 柠檬酸化学式 Buy 柠檬酸化学式 无水柠檬酸 柠檬酸一水合物product On Alibaba Com
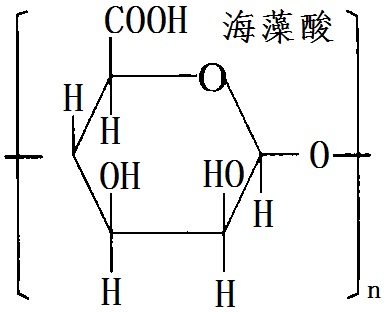



海藻酸cas 9005 32 7
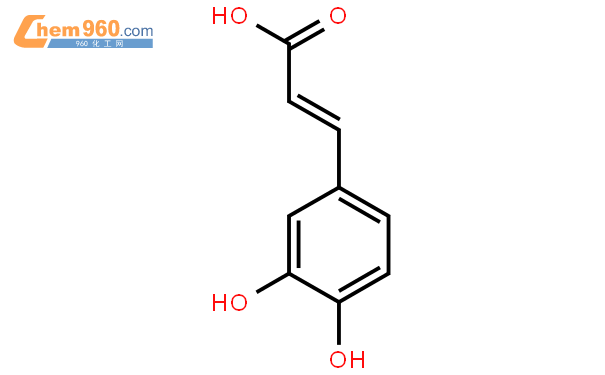



咖啡酸结构式 咖啡酸化学式 960化工网




柠檬酸化学式2 羟基丙烷 1 2 3 三羧酸柑橘 乙酸乙酯png图片素材免费下载 图片编号 Png素材网
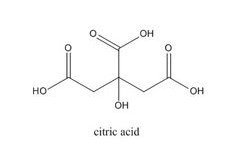



360百科




戊二酸的化学式 金腾龙



蒽酸化学式分子式化合物 化合物png图片素材免费下载 图片编号 Png素材网



柠檬酸
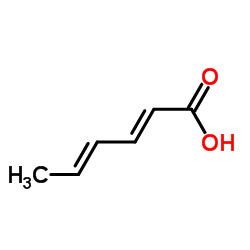



山梨酸 Msds 用途 密度 山梨酸cas号 110 44 1 化源网



亚油酸 Linoleic Acid 60 33 3 参数 分子结构式 图谱信息 物竞化学品数据库 专业 全面的化学品基础数据库




中国供应商直接销售化学式硅酸钠 Buy 化学式硅酸钠 硅酸钠机 水玻璃炉product On Alibaba Com



脂肪酸甘油和脂肪酸的化学式 大业商务网



常见含氧酸结构式的写法 常见含氧酸化学式 慕舍网




邻苯二甲酸二酯化学式 邻苯二甲酸二酯毒性与危害 帝思创
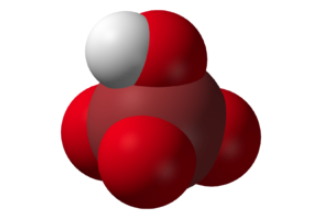



高溴酸



氯酸钠 氯酸钠是什么 化学式 多少钱一吨 恒亿化工



有机酸的分子式 所有有机酸的化学式 手机问答网



2 2 二羟甲基丁酸化学式 上海金腾龙




化学物质化学异烟酸化学式羧酸酰肼png图片素材免费下载 图片编号 Png素材网
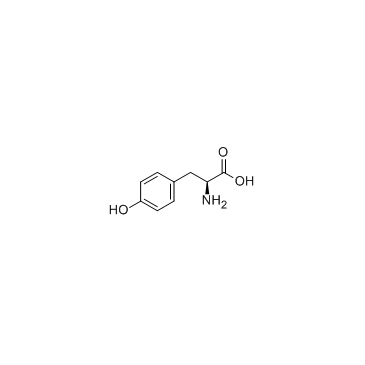



L 酪氨酸 Msds 用途 密度 L 酪氨酸cas号 60 18 4 化源网




高锰酸钾化学式 三顶新知



氯酸钠 氯酸钠是什么 化学式 多少钱一吨 恒亿化工



丙酸 Wikiwand



磷钨酸 专业钨酸盐生产商和供应商 中钨在线



酸的化学式 初三网




次氟酸 维基百科 自由的百科全书




硬脂酸结构式 硬脂酸化学式 960化工网
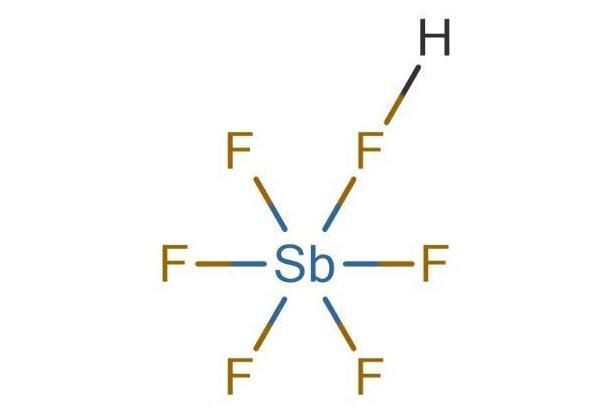



氟锑酸 无机化合物 搜狗百科
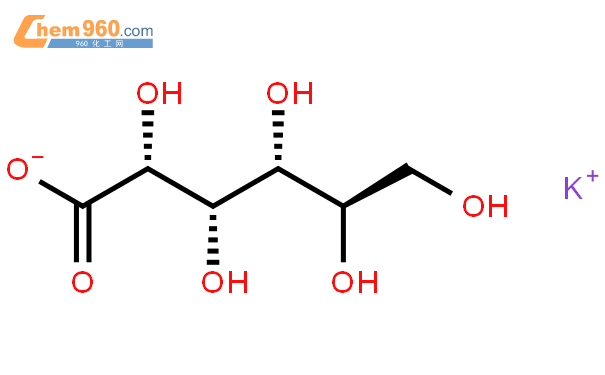



葡萄糖酸钾结构式 葡萄糖酸钾化学式 960化工网




写出三酸两碱的化学式盐酸 硫酸 硝酸 Hcl H2so4 Hno3 氢氧化钙 氢氧化钠 Ca Oh 2 Naoh Ppt Download
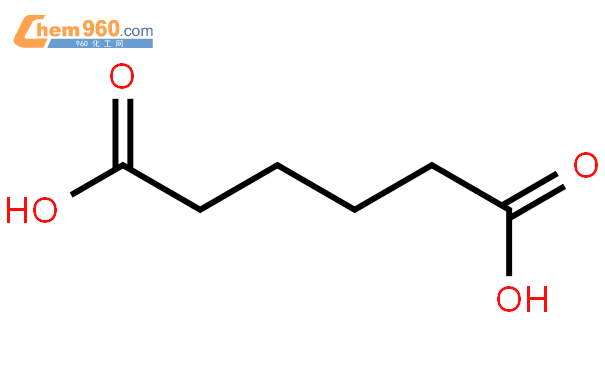



己二酸结构式 己二酸化学式 羟基己二酸结构式 北庭网



中考化学专题复习测试卷有关化学式的计算 试卷后含答案 好学电子课本网



氯水的化学式氯水的化学式是什么 新绅网




高锰酸钾的化学式高锰酸钾化学式怎么写



水杨酸 简介 作用 危害 结构式 化学式 毒理 合成 范德生物科技公司



維a酸 维基百科 自由的百科全书



初中有机酸化学式 所有有机酸的化学式 手机问答网



常见有机酸化学式 所有有机酸的化学式 手机问答网



1



常用的有机酸有哪些 常见有机酸化学式 手机问答网



氯化氢的化学式氯化氢的化学式是 一加一
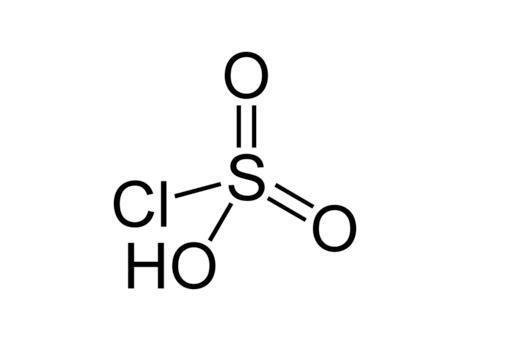



氯磺酸 搜狗百科



硅钨酸化学式图片 0018 中钨图秀网



柠檬酸 Citric Acid 77 92 9 参数 分子结构式 图谱信息 物竞化学品数据库 专业 全面的化学品基础数据库




强酸有哪些化学式 Seo Sem 站长 知道 Shong



水杨酸 简介 作用 危害 结构式 化学式 毒理 合成 范德生物科技公司
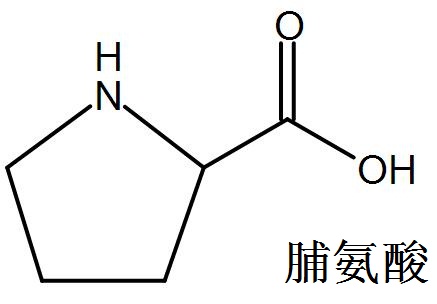



脯胺酸化學式 Neovid




硬脂酸 Msds 用途 密度 硬脂酸cas号 57 11 4 化源网




含氧酸記憶方法 凡鳥手札
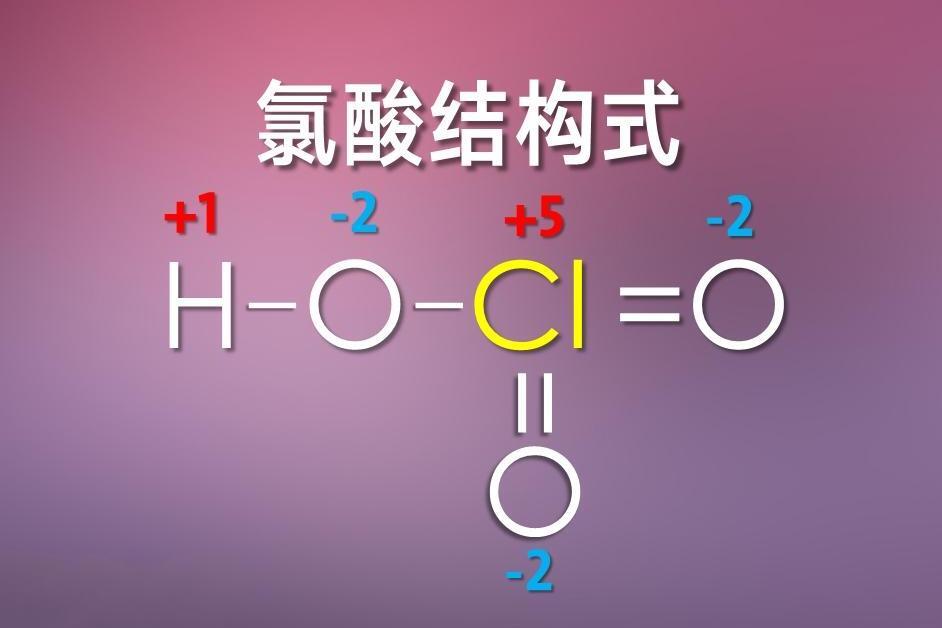



氯酸 搜狗百科



硬化油化学式硬脂酸 软脂酸 油酸的化学式是什么 银颜网



镁与稀硫酸的反应化学式 华中教育资源网
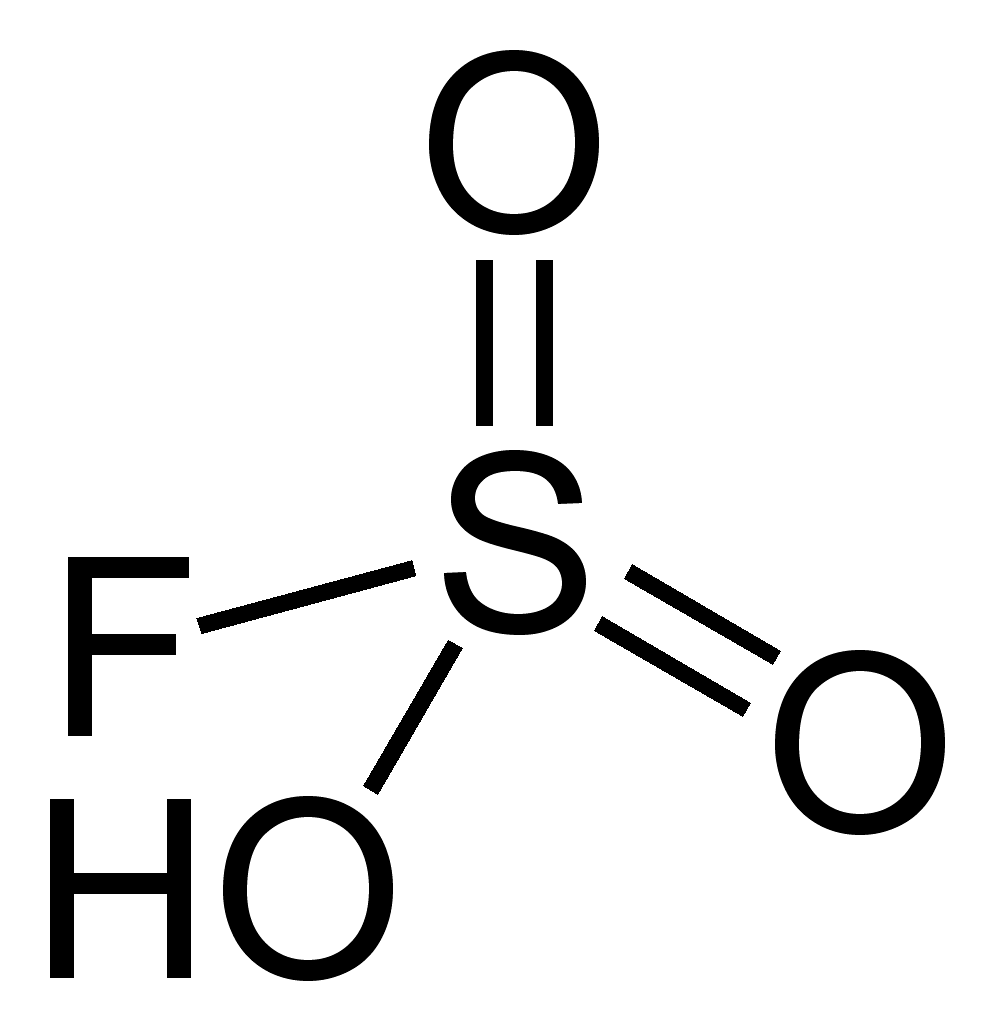



氟磺酸 维基百科 自由的百科全书



科普知识 次氯酸 重庆鑫鹏健康科技有限公司




科普下硅酸钠是什么化学式怎么写 环球信息网




详细说明氯酸钠化学式为naclo3 相对分子质量106 44 通常为白色或微黄色等轴晶体 地一眼



较真丨果酸 水杨酸 A酸 刷酸真的能 换肤 吗 腾讯新闻



硬脂酸 Stearic Acid 57 11 4 参数 分子结构式 图谱信息 物竞化学品数据库 专业 全面的化学品基础数据库
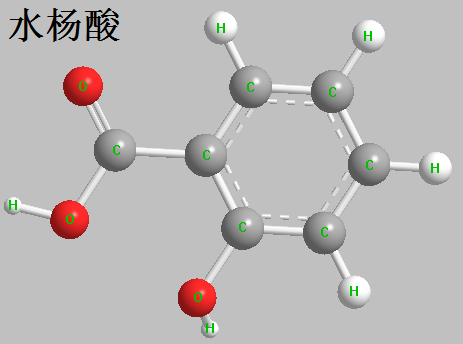



水杨酸 69 72 7



0 件のコメント:
コメントを投稿